
Descubre los secretos del cerebro y la investigación en epilepsia que se lleva a cabo en el Hospital Sant Joan de Déu Barcelona.
Nuestro cerebro es un órgano complejo que procesa grandes cantidades de información. En determinadas ocasiones, sus conexiones no funcionan correctamente, pudiendo originar lo que conocemos como crisis epilépticas. A través de los materiales divulgativos del Ágora de la Ciencia podrás indagar sobre cómo funciona el cerebro humano y conocer los últimos avances en el estudio y tratamiento de la epilepsia realizados en el Hospital Sant Joan de Déu.
SJD Investiga
En el Hospital Sant Joan de Déu Barcelona investigamos enfermedades que afectan a niños y niñas en edad pediátrica. Apostamos por la investigación traslacional, aquella que busca trasladar al paciente la investigación biomédica básica que se inicia en el laboratorio, generando así conocimiento para el desarrollo de tratamientos innovadores.
Nuestros equipos investigadores trabajan para conocer en mayor profundidad la epilepsia que aparece en la edad pediátrica (su origen, los mecanismos biológicos que la desencadenan o su relación con diversas mutaciones) y también para mejorar su diagnóstico.
Proyectos de investigación en epilepsia infantilEstudio comparativo de pruebas de neuroimagenEl objetivo de este estudio era comparar diferentes tipos de pruebas de neuroimagen para averiguar cuál determina con mayor precisión la zona en la que se generan las crisis epilépticas focales. Esto ayudará a los profesionales médicos a realizar cirugías más dirigidas.
Más informaciónSJD InvestigaEstudio de pruebas de neuroimagen
Hemos realizado un estudio con el objetivo de identificar pruebas de neuroimagen que determinen con mayor precisión la zona en la que se generan las crisis epilépticas focales para realizar cirugías más dirigidas.
Cirugía para tratar la epilepsia
En ocasiones, en aquellos casos en los que la epilepsia no responde al tratamiento farmacológico, se recomienda realizar una cirugía, ya que se ha visto que en 2 de cada 3 casos se consigue una reducción importante de las crisis (más del 90%) o incluso una ausencia de convulsiones. El control temprano de las crisis es fundamental para evitar retrasos en el neurodesarrollo.
Estudio comparativo de pruebas de neuroimagen: ¿Cuál identifica con mayor precisión la zona del cerebro en la que se produce la crisis epiléptica?
Se ha evaluado y comparado la utilidad de PISCOM, una nueva técnica de neuroimagen, con SISCOM y 18F-FDG PET, otras técnicas complementarias que se utilizan para evaluar la zona epileptógena. Esta zona es el área de tejido cerebral necesario para que se origine una crisis epiléptica. Su extracción provoca una supresión de las crisis.
Visita la sala de diagnóstico y mapeo cerebral del Hospital Sant Joan de Déu:
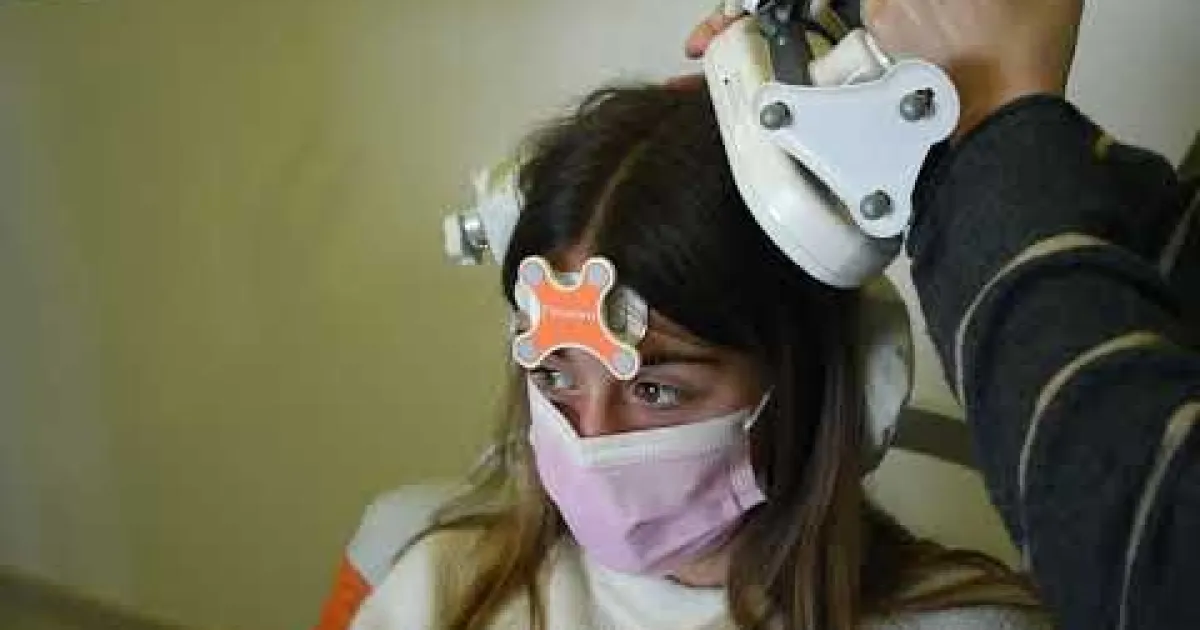 https://www.youtube.com/watch?v=1kQh_8DFpoM
https://www.youtube.com/watch?v=1kQh_8DFpoM Estudio de las GRINpatíasHemos estudiado de manera individualizada el efecto que tienen algunas mutaciones en genes GRIN de pacientes pediátricos sobre el receptor NMDA, un receptor del neurotransmisor glutamato localizado en la membrana de las neuronas.
Más informaciónSJD InvestigaEstudio de las GRINpatías
Hemos estudiado de manera individualizada el efecto de diferentes mutaciones de niños y niñas con GRINpatías (trastornos raros del neurodesarrollo) sobre el receptor NMDA, un receptor del neurotransmisor glutamato localizado en la membrana neuronal. La función del receptor NMDA está alterada en estos pacientes a causa de mutaciones en los genes GRIN.

La función de los receptores de glutamato de tipo NMDA, proteínas implicadas en la sinapsis neuronal, puede verse alterada por mutaciones en los genes GRIN, dando lugar a unos trastornos denominados GRINpatías.
¿Qué es la sinapsis neuronal? Este concepto hace referencia al espacio que hay entre neurona y neurona, a través del cual se transmite el impulso nervioso. Cuando hay alguna alteración en la sinapsis las neuronas del cerebro tienen dificultades para comunicarse entre ellas y con las células de otras partes de nuestro cuerpo, causando enfermedades y/o trastornos neurológicos.
Las GRINpatías alteran el correcto desarrollo del cerebro y pueden producir crisis epilépticas. Es crucial conocer el impacto de las mutaciones de los genes GRIN sobre el funcionamiento del receptor de glutamato de tipo NMDA con el fin de explorar posibles tratamientos.
Estudio del impacto funcional de mutaciones de los genes GRIN, causantes de alteraciones de los receptores de glutamato de tipo NMDA
A través de un modelo estructural 3D del receptor NMDA y otro tipo de estudios, se ha estudiado qué sintomatología concreta producen diversas mutaciones en los genes GRIN. Además, este modelo 3D también permite investigar posibles tratamientos.
En esta línea, se ha empleado la técnica "patch-clamp" para estudiar más a fondo qué tipo de cambios producen las diversas mutaciones GRIN en el funcionamiento del receptor NMDA. ¡Te la explicamos a través de un vídeo!
La técnica del "patch-clamp"
 https://www.youtube.com/watch?v=z_dfBQeRTvw
https://www.youtube.com/watch?v=z_dfBQeRTvw Estudio de canalopatías de tipo KCNQ2Este estudio tenía como objetivo la búsqueda de marcadores de la canalopatía de tipo KCNQ2, así como el estudio de su sintomatología, que incluye la epilepsia, y el análisis del efecto de tratamientos que actúan sobre los canales mutados.
Más informaciónSJD InvestigaEstudio de las canalopatías
Para conocer más en detalle la canalopatía de tipo KCNQ2, hemos estudiado qué síntomas concretos producen las diversas mutaciones que pueden causarla (incluida la epilepsia) y hemos analizado el efecto de tratamientos que actúan sobre los canales iónicos mutados. Las canalopatías de tipo KCNQ2 son trastornos neurológicos producidos por diferentes mutaciones en el gen KCNQ2, que codifica para un canal iónico localizado en las neuronas cerebrales relacionado con el paso de potasio a través de las mismas.
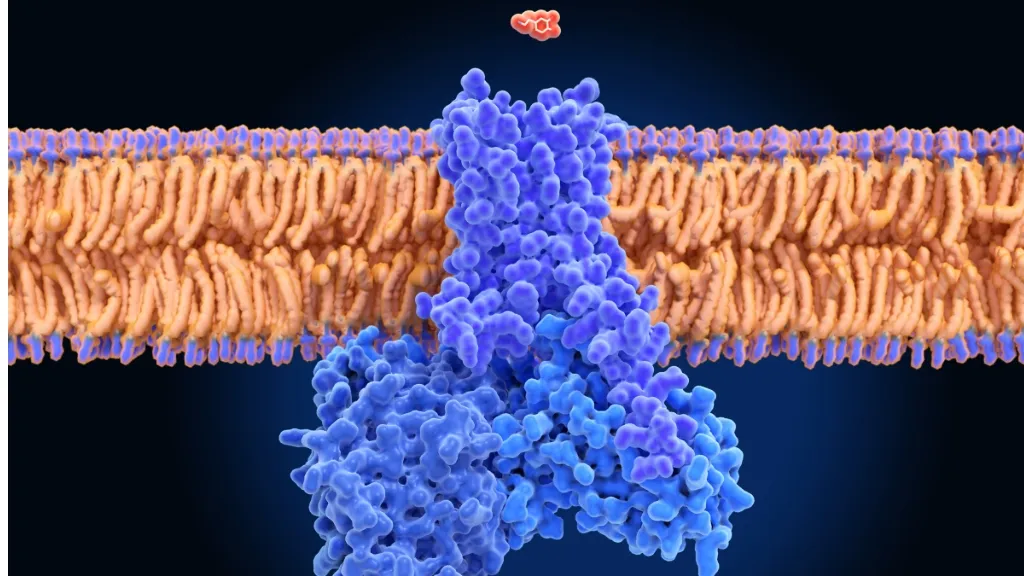
Mutaciones en los canales de la membrana neuronal
La membrana neuronal tiene una serie de proteínas que actúan como canales que posibilitan la circulación de los iones. Los iones participan en la transmisión del impulso nervioso (señal que se transmite de una neurona a otra y que permite enviar información a las células del cuerpo).
Algunas mutaciones generan una actividad anómala de estos canales, repercutiendo en el funcionamiento de la sinapsis neuronal (espacio que existe entre neurona y neurona, a través del que pasan los impulsos nerviosos, y que permite la comunicación entre ellas). Estas alteraciones, conocidas como canalopatías, pueden causar epilepsia y otros síntomas neurológicos. Es fundamental saber, por un lado, cómo afecta al cerebro de los recién nacidos cada mutación de los genes que codifican para estos canales, y por otro, cómo influye la epilepsia en su neurodesarrollo. También es importante probar qué tratamientos funcionan mejor en cada caso concreto.
Proyecto BIO-KCNQ2. Estudio de la canalopatía KCNQ2: análisis de biomarcadores, efectos de las mutaciones y evaluación de la eficacia de los tratamientos
Se ha realizado estudios genéticos a un grupo de niños y niñas para detectar mutaciones en el gen KCNQ2 que provocan epilepsia. También se han realizado pruebas neurológicas y se han aplicado escalas médicas para describir la sintomatología y los problemas en el neurodesarrollo que causa cada mutación. Finalmente, se han proporcionado diversos fármacos a los pacientes para conocer su efecto en cada caso concreto.
El objetivo de este estudio era comparar diferentes tipos de pruebas de neuroimagen para averiguar cuál determina con mayor precisión la zona en la que se generan las crisis epilépticas focales. Esto ayudará a los profesionales médicos a realizar cirugías más dirigidas.
Estudio de pruebas de neuroimagen
Hemos realizado un estudio con el objetivo de identificar pruebas de neuroimagen que determinen con mayor precisión la zona en la que se generan las crisis epilépticas focales para realizar cirugías más dirigidas.

Cirugía para tratar la epilepsia
En ocasiones, en aquellos casos en los que la epilepsia no responde al tratamiento farmacológico, se recomienda realizar una cirugía, ya que se ha visto que en 2 de cada 3 casos se consigue una reducción importante de las crisis (más del 90%) o incluso una ausencia de convulsiones. El control temprano de las crisis es fundamental para evitar retrasos en el neurodesarrollo.
Estudio comparativo de pruebas de neuroimagen: ¿Cuál identifica con mayor precisión la zona del cerebro en la que se produce la crisis epiléptica?
Se ha evaluado y comparado la utilidad de PISCOM, una nueva técnica de neuroimagen, con SISCOM y 18F-FDG PET, otras técnicas complementarias que se utilizan para evaluar la zona epileptógena. Esta zona es el área de tejido cerebral necesario para que se origine una crisis epiléptica. Su extracción provoca una supresión de las crisis.
Visita la sala de diagnóstico y mapeo cerebral del Hospital Sant Joan de Déu:

Hemos estudiado de manera individualizada el efecto que tienen algunas mutaciones en genes GRIN de pacientes pediátricos sobre el receptor NMDA, un receptor del neurotransmisor glutamato localizado en la membrana de las neuronas.
Estudio de las GRINpatías
Hemos estudiado de manera individualizada el efecto de diferentes mutaciones de niños y niñas con GRINpatías (trastornos raros del neurodesarrollo) sobre el receptor NMDA, un receptor del neurotransmisor glutamato localizado en la membrana neuronal. La función del receptor NMDA está alterada en estos pacientes a causa de mutaciones en los genes GRIN.

La función de los receptores de glutamato de tipo NMDA, proteínas implicadas en la sinapsis neuronal, puede verse alterada por mutaciones en los genes GRIN, dando lugar a unos trastornos denominados GRINpatías.
¿Qué es la sinapsis neuronal? Este concepto hace referencia al espacio que hay entre neurona y neurona, a través del cual se transmite el impulso nervioso. Cuando hay alguna alteración en la sinapsis las neuronas del cerebro tienen dificultades para comunicarse entre ellas y con las células de otras partes de nuestro cuerpo, causando enfermedades y/o trastornos neurológicos.
Las GRINpatías alteran el correcto desarrollo del cerebro y pueden producir crisis epilépticas. Es crucial conocer el impacto de las mutaciones de los genes GRIN sobre el funcionamiento del receptor de glutamato de tipo NMDA con el fin de explorar posibles tratamientos.
Estudio del impacto funcional de mutaciones de los genes GRIN, causantes de alteraciones de los receptores de glutamato de tipo NMDA
A través de un modelo estructural 3D del receptor NMDA y otro tipo de estudios, se ha estudiado qué sintomatología concreta producen diversas mutaciones en los genes GRIN. Además, este modelo 3D también permite investigar posibles tratamientos.
En esta línea, se ha empleado la técnica "patch-clamp" para estudiar más a fondo qué tipo de cambios producen las diversas mutaciones GRIN en el funcionamiento del receptor NMDA. ¡Te la explicamos a través de un vídeo!
La técnica del "patch-clamp"

Este estudio tenía como objetivo la búsqueda de marcadores de la canalopatía de tipo KCNQ2, así como el estudio de su sintomatología, que incluye la epilepsia, y el análisis del efecto de tratamientos que actúan sobre los canales mutados.
Estudio de las canalopatías
Para conocer más en detalle la canalopatía de tipo KCNQ2, hemos estudiado qué síntomas concretos producen las diversas mutaciones que pueden causarla (incluida la epilepsia) y hemos analizado el efecto de tratamientos que actúan sobre los canales iónicos mutados. Las canalopatías de tipo KCNQ2 son trastornos neurológicos producidos por diferentes mutaciones en el gen KCNQ2, que codifica para un canal iónico localizado en las neuronas cerebrales relacionado con el paso de potasio a través de las mismas.

Mutaciones en los canales de la membrana neuronal
La membrana neuronal tiene una serie de proteínas que actúan como canales que posibilitan la circulación de los iones. Los iones participan en la transmisión del impulso nervioso (señal que se transmite de una neurona a otra y que permite enviar información a las células del cuerpo).
Algunas mutaciones generan una actividad anómala de estos canales, repercutiendo en el funcionamiento de la sinapsis neuronal (espacio que existe entre neurona y neurona, a través del que pasan los impulsos nerviosos, y que permite la comunicación entre ellas). Estas alteraciones, conocidas como canalopatías, pueden causar epilepsia y otros síntomas neurológicos. Es fundamental saber, por un lado, cómo afecta al cerebro de los recién nacidos cada mutación de los genes que codifican para estos canales, y por otro, cómo influye la epilepsia en su neurodesarrollo. También es importante probar qué tratamientos funcionan mejor en cada caso concreto.
Proyecto BIO-KCNQ2. Estudio de la canalopatía KCNQ2: análisis de biomarcadores, efectos de las mutaciones y evaluación de la eficacia de los tratamientos
Se ha realizado estudios genéticos a un grupo de niños y niñas para detectar mutaciones en el gen KCNQ2 que provocan epilepsia. También se han realizado pruebas neurológicas y se han aplicado escalas médicas para describir la sintomatología y los problemas en el neurodesarrollo que causa cada mutación. Finalmente, se han proporcionado diversos fármacos a los pacientes para conocer su efecto en cada caso concreto.














